[팜뉴스=김민건 기자] EGFR 변이 비소세포폐암 1차치료에 타그리소(오시머티닙)를 사용했을 때 임상 연구와 달리 실제 전체생존기간 중앙값(mOS)이 짧다는 결과가 발표돼 업계 이목을 끌고 있다. 글로벌 3상 연구 FLAURA 임상 참여 기준을 충족하는 환자와 미충족 환자군을 나눠 비교한 결과인데 FLAURA는 EGFR 변이 비소세포폐암 1차치료에 타그리소를 투여하는 핵심 근거 연구다.
12일 국제학술지 Lung cancer에는 'BC 암 연구소 밴쿠버 센터(BC Cancer Agency Vancouver Centre)'가 발표한 타그리소 리얼월드데이터 분석 결과가 올라와 있다.
타그리소는 FLAURA 임상을 토대로 EGFR 변이 폐암 1차치료에 사용 중이다. 이 연구에서 타그리소는 백금기반 항암화학요법과 비교 평가를 통해 전체생존기간 중앙값 38.6개월을 기록하는 등 성과를 냈다.
그러나 실제 환자 치료는 임상 결과와 다른 경우가 많다는 게 이 연구의 배경이다. 연구진은 "항암 치료제는 일상 진료 현장에서 보는 것과 다른 경우가 많다"며 "임상에서는 건강 상태가 좋지 않거나 동반 질환이 있는 환자를 제외한다"고 설명했다.
이어 "임상 참여 자격이 있는 환자보다는 자격을 충족하지 못한 환자에서 생존율이 떨어지는 것으로 나타났다"며 "현재까지 리얼월드에서 (1차치료에) 타그리소 효능을 평가한 데이터는 제한적으로, 진행성 폐암 환자 40% 이상이 ECOG(European Cooperative Oncology Group) 0~1등급이지만 FLAURA 임상에서는 2등급 이하로 환자 등록을 제한했다"며 배경을 밝혔다.
이에 연구진은 캐나다에서 전이성 EGFR 엑손19 또는 L858R 변이가 있는 환자에게 1차 치료제로 타그리소를 사용했을 때 전체생존기간 중앙값(mOS)을 분석했다. FLAURA 기준에 맞는 환자와 그렇지 못한 환자 총 311명을 통해 임상과 달리 통제되지 않은 현실에서 효과를 보고자 한 것이다.
환자들은 2020년 1월부터 2021년 10월까지 타그리소를 사용해 치료했으며 임상 참여 제한 기준으로 앞서 언급된 ECOG 2점 이상, 뇌전이나 스테로이드 투약, 헤모글로빈 수치 90g/L 이하, 혈소판 100x10^9/L(10만개 미만) 이하, 크레아티닌 혈청 수치 50mL/min 등을 설정했다. 실제 FLAURA 임상에 적용한 환자 참여 기준이기도 하다.
ECOG는 환자의 신체 능력을 평가하는 것으로 0점(무증상), 1점(약간의 증상), 2점(증상이 있으며 낮 시간의 절반을 침대에서 보냄), 3점(낮 시간대 절반 이상을 침대에서 보냄), 4점(하루 종일 누워 지냄)으로 분류한다. 2점 이상은 정상적인 일상을 보낼 수 없는 상태로 수술을 권하지 않는다. 3점부터는 증상 완화 목적 치료 외에 권하지 않는 상태다.

뇌 전이·스테로이드 사용 환자, 헤모글로빈 수치가 90g/L 미만인 경우 정상적인 치료를 받기에 위험할 수 있다. 혈소판 수치가 10만개 미만이거나 크레아티닌 혈청 수치가 낮아도 심각한 부작용을 겪을 수 있어 임상에 참여하기에는 부적합하다.
연구진은 이러한 기준에 따라 FLAURA 임상에 참여할 수 있었던 환자, 참여할 수 없었던 환자를 나눴고 311명 중 137명(44%)을 FLAURA 임상 부적합 환자로 분류, 다시 120명은 ECOG 수행 점수에 따라 부적합으로 판단했다.
300명 수준 규모 리얼월드이지만 실제 진료 현장에서 1차치료에 타그리소를 처방받은 환자를 분석한 결과, 절반은 FLAURA 연구에 참여할 수 없는 상태로 나타난 것이다. 이번 연구를 통해 실제적인 타그리소의 생존 혜택을 보고자 한 이유다.
리얼월드데이터를 분석해보니 타그리소를 1차치료부터 사용하더라도 FLAURA 임상과 달리 실제 진료 현장에서는 전체생존기간 중앙값이 18개월 정도 차이가 나는 것을 확인했다.
좀더 자세히 추적관찰 중앙값 26.5개월 시점에 전체 환자 311명(FLAURA 임상 적합·부적합 모두 포함)의 전체생존기간 중앙값(mOS)은 전체 환자군에서 27.4개월, FLAURA 임상 부적합 환자군 15.8개월, 임상 적합 환자군 34.2개월을 보였다. 임상 적합군과 부적합 군에서 전체생존 데이터가 1년 이상 차이를 보였다.
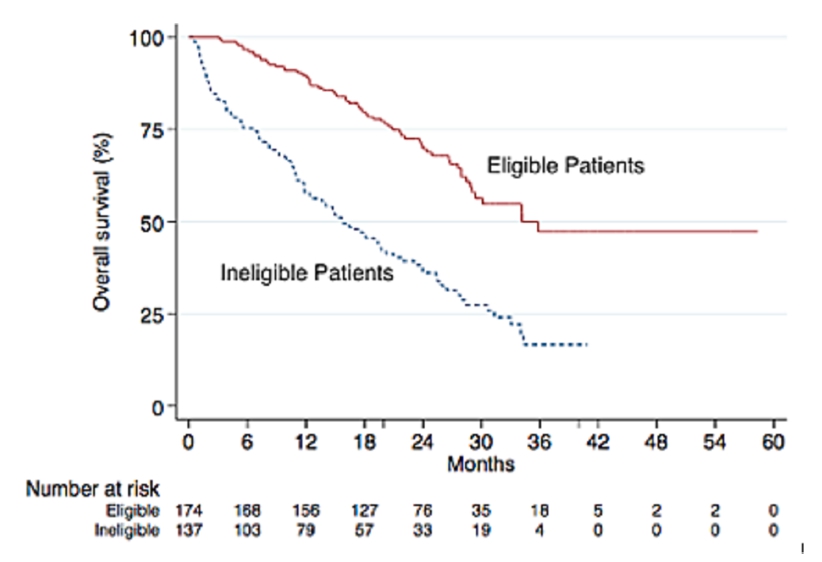
FLAURA 임상에서 전체생존기간 중앙값은 38.6개월이었다. 임상에 적합한 환자군은 실제 치료를 받아도 34.2개월로 비슷한 기간을 나타냈지만, 임상 부적합 환자군은 타그리소 1차치료 효과가 상대적으로 떨어진다는 분석이다.
다만, 연구진은 "이번 연구가 실제 진료 환경에서 전체생존 데이터를 보고한 가장 큰 규모의 데이터지만 한계점이 있다"고 강조했다. 연구진은 "부적합 환자군에서 4기, 4B기, 3개 이상의 전이, L858R 변이가 있는 비율이 높았다"면서 "임상에 부적합한 환자들은 기저 시점에서 질병 부담이 더 높았기 때문에 결과가 안 좋았을 수 있다"고 추측했다.
또한 연구진은 "대부분 환자의 ECOG 수행 상태가 좋지 않아 부적합으로 간주했으며 다른 제외 기준에 대한 하위 그룹 분석이 불가능했다"며 "임상 부적합 환자군에서 1·2세대 EGFR-TKI 억제제 효능 데이터가 부족했고, 최선의 지지요법(BSC)을 진행한 환자에서 결과도 부족해 다른 치료 옵션과 타그리소를 비교하는 결론을 내릴 수 없었다"고 했다.
그러면서 FLAURA 임상 부적합군처럼 예후가 좋지 않은 환자들의 치료 성적을 개선하기 위해 더 많은 연구가 필요하다고 강조했다. 최근 발표된 EGFR 변이 비소세포폐암 1차치료에서 타그리소+백금기반 항암화학요법, 렉라자(레이저티닙)+리브리반트(아미반타맙) 병용요법에 대한 기대와 우려를 표했다.
연구진은 "최근 FLAURA2에서 (1차치료에서)타그리소와 백금기반 항암화학요법 병용 시 타그리소 단독 요법 대비 무진행생존기간을 개선했다"며 "렉라자와 리브리반트 병용도 타그리소 단독요법 대비 우수한 무진행생존기간을 보였다"고 설명했다. 그러나 "두 임상 모두 적절한 건강 상태를 가진 환자로 제한했고 많은 항암 연구자들이 독성 증가 우려로 임상적으로 건강하지 않은 환자에서 병용 치료를 주저할 수 있다"고 밝혔다.
관련기사
개의 댓글
댓글 정렬
그래도 삭제하시겠습니까?

