[팜뉴스=김민건 기자] 최초의 GIP·GLP-1 수용체작용제 '마운자로(성분명 터제파타이드)'가 성인 제2형 당뇨병 치료제로 국내 허가를 받았다.
28일 한국릴리(대표 크리스토퍼 제이 스톡스)는 식품의약품안전처로부터 마운자로 단독요법 및 병용요법 시 성인 제2형 당뇨병 환자 혈당 개선을 위한 식이 요법과 운동 요법 보조제로 승인 받았다며 이같이 밝혔다.
국내 허가 용량은 2.5mg, 5mg, 7.5mg, 10mg, 12.5mg, 15mg으로 총 6가지다.
마운자로는 인슐린 분비를 증가시키는 대표적인 인크레틴 호르몬인 GIP(glucose-dependent insulinotropic polypeptide)와 GLP-1(glucagon-like peptide-1) 수용체를 모두 활성화시키는 단일 분자다.
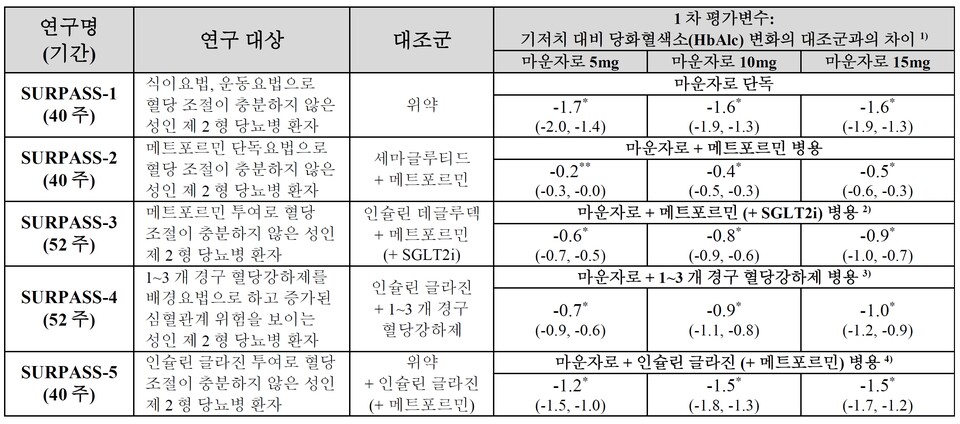
마운자로의 국내 허가는 제2형 당뇨병 환자를 대상으로 5개의 무작위 배정, 이중맹검, 다기관 3상인 SURPASS 연구를 통해 확인한 위약, 세마글루티드(1mg), 인슐린 데글루덱(100U/mL), 인슐린 글라진(100U/mL) 대비 마운자로(5, 10, 15mg) 단독요법 또는 병용요법의 유효성 및 안전성 프로파일을 기반으로 이루어졌다.
1차 평가변수는 기저치(baseline) 대비 당화혈색소(HbAlc)의 평균 변화였다. 마운자로는 체중 감소를 위한 치료제로 허가 받지 않았으며, 체중 변화량은 SURPASS 연구의 주요 2차 평가변수로 평가했다.
SURPASS 연구 결과 마운자로는 대조군 대비 통계적으로 유의하게 당화혈색소(HbA1c)를 감소시켰다. 마운자로 5mg 투여군의 당화혈색소(HbAlc)는 평균적으로 기저치 대비 1.8~2.1% 감소했으며, 10mg 또는 15mg 투여군의 당화혈색소(HbAlc)는 평균적으로 기저치 대비 1.7~2.4% 감소한 것으로 확인됐다.
마운자로 유효성은 연령, 성별, 인종, 민족, 지역, 체질량지수(BMI), 당화혈색소(HbAlc), 당뇨병 유병 기간, 신기능에 따른 영향을 받지 않았다.
한편, 한국릴리는 마운자로 임상에서 가장 빈번하게 보고된 이상반응은 오심, 설사, 구토를 포함한 위장관 장애였다고 밝혔다. 이러한 반응의 중증도는 경증 또는 중등증이었고, 용량 증량 중에 더 자주 발생했으며, 시간이 경과함에 따라 감소했다.
키워드
#마운자로관련기사
개의 댓글
댓글 정렬
그래도 삭제하시겠습니까?

