[팜뉴스=김민건 기자] 유방암 치료 난제인 전이성 삼중음성 유방암(advanced triple-negative breast cancer, 이하 TNBC) 환자를 살릴 수 있는 또 다른 치료제가 등장했다. 길리어드 사이언스의 야심작 '트로델비(사시투주맙 고비테칸)'다.
10일 탁산(taxane) 계열 세포독성항암제에 재발·불응하는 삼중음성 유방암에 항체약물접합체(Antibody-Drug Conjugate, ADC) 신약 트로델비가 공식 허가돼 처방권에 들어왔다.
면역항암제, PARP 저해제 이후 등장한 새로운 기전의 신약인 만큼 전이성 TNBC 유방암 생존 연장에 보일 실제 효과가 궁금하지 않을 수 없다.
긍정적인 부분은 임상 연구에서 세포독성항암제 단독 요법 대비 무진행생존기간(Progression free-survival, PFS)과 전체생존기간(Overall survival, OS)을 단 몇 개월이라도 개선한 만큼 현재까지 평가는 '효과적'이라고 말할 수 있다.
트로델비의 성공은 항암제 개발에 역량을 쏟고 있는 길리어드에 '에이즈 치료 명가'라는 이름 외에 새로운 명성을 안겨줄지 모른다.
▶공격적인 유방암 'ER, PR, HER2 음성'에 등장한 ADC 신약
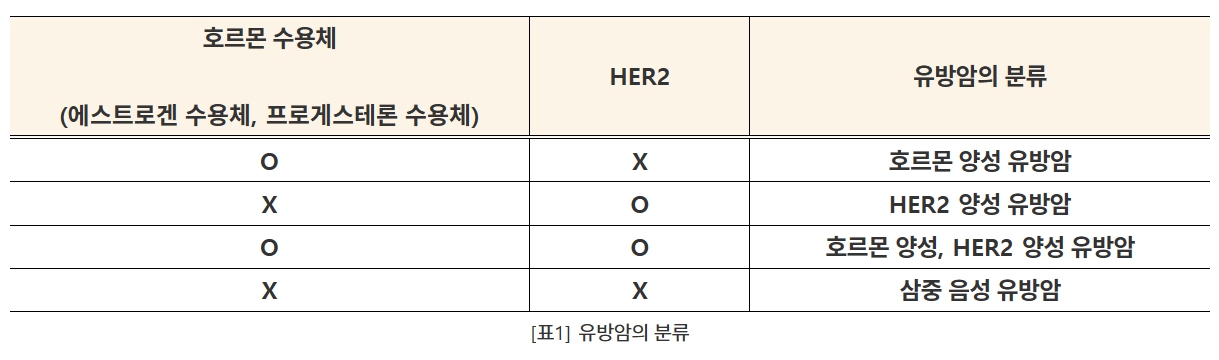
유방암 환자를 면역조직화학 염색(IHC)으로 진단하면 ER·PR 호르몬 양성(65%), HER2 양성(15~20%), TNBC( 15%) 순으로 확인된다.
전체 유방암 환자에서 적지 않은 비중을 차지하는 TNBC는 고분화, 진행성, 재발이 특징으로 가장 공격적인 암종이다. 이 때문에 조기(1~2기) 진단 환자 절반은 1~2년 이내 재발을 경험할 만큼 진행이 빠르고, 많은 경우 3~4기에 진단받아 5년 상대생존율은 30%로 낮다.
이름에서 보듯 에스트로겐 수용체(estrogen receptors, ER), 프로게스테론 수용체(progesterone receptors, PR)가 발현되지 않아 아로마타제 억제제 같은 호르몬 치료에 효과가 없으며, HER2 수용체도 발현하지 않아 허셉틴, 퍼제타 등 표적치료에도 반응하지 않기 때문이다.
이에 전이성 TNBC 치료는 세포독성항암제에 의존해야 했다. 독소루빈신(Doxorubicin) 등 안트라사이클린 계열과 도세탁셀(docetaxel), 파클리탁셀(paclitaxel) 등 탁산 계열이다. 이 경우 전체생존기간 중앙값은 1년이 되지 못했다.
새롭게 PARP 저해제 린파자(아스트라제네카, 올라파립)와 면역항암제 키트루다(MSD, 펨브롤리주맙)가 등장하며 1년 이상 생존 혜택을 보였지만 보험급여 적용 등 문제가 있다.
그렇기 때문에 전이성 TNBC는 1차 치료 이후 낮은 반응률과 짧은 무진행 생존기간을 가진 세포독성항암제를 표준요법으로 써야 했다. 새로운 치료제 개발이 요구돼 왔고 지난 2020년 길리어드가 항암제 개발 전문 기업 이뮤노메딕스를 210억달러에 인수하며 트로델비 개발에 나선 까닭이기도 하다.
▶첫 TROP-2 표적 신약으로 등장한 트로델비
트로델비는 처음으로 개발된 TROP-2 표적 항체약물접합체(Antibody-Drug Conjugate, ADC)로 세포표면항원 TROP-2에 결합하는 단클론항체와 강력한 세포사멸 기능을 갖는 DNA 회전효소 억제 약물(TOP1 inhibitor payload) SN-38로 구성된다.
항원 TROP-2는 유방암 (90% 이상)을 포함한 다양한 암종에서 고밀도로 발현한다. 암세포 표면에 발현된 Trop-2 항원을 추적한 트로델비는 내부로 들어가 세포독성 약물인 SN-38을 뿌리게 된다. 암세포 안에서 항체, 링커와 끊어진 SN-38은 주변에 있는 암까지 공격하는 부가적 효과도 가진다.
이러한 효과를 처음으로 확인한 연구가 전이성 TNBC 환자 108명을 대상으로 한 트로델비 단독 투여 1·2상 'IMMU-132-01'이다. 트로델비는 객관적 반응률(ORR) 33%, 무진행 생존기간(PFS) 5.5개월, 전체 생존기간(OS) 12개월을 나타냈으며 미국 FDA는 지난 2020년 가속승인(accelerated approval)에 올려 허가한 뒤 이듬해 4월 글로벌 3상 'ASCENT' 연구를 토대로 최종 승인했다.
▶ASCENT 임상 17.7개월 시점에 효과 입증으로 중단 권고
ASCENT 연구를 통해 트로델비와 항암화학요법 단독 투여를 비교한 결과 무진행생존기간과 전체생존기간에서 뛰어나다는 점이 입증됐다. 트로델비 항암 반응은 면역관문억제제(PD-1 또는 PD-L1) 투여 환자와 뇌전이 환자에서도 확인하며 의미를 더했다.
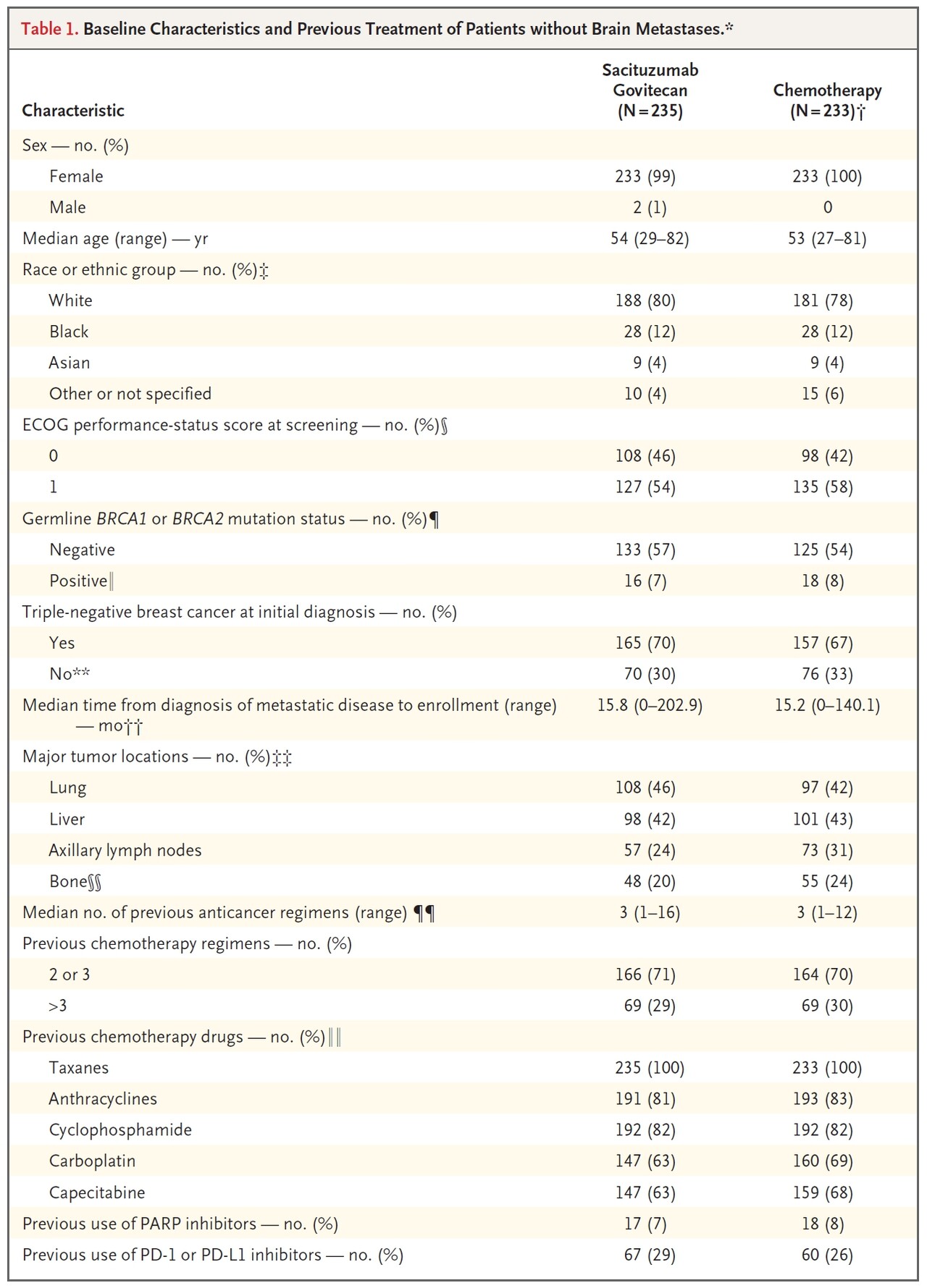
연구는 2017년 11월부터 2019년 9월까지 7개국 88개 병원에서 앞서 탁산 계열 항암제를 포함한 두 개 이상의 표준항암화학요법에도 재발 또는 전이성인 TNBC 환자 총 529명을 등록, 분석했다.
트로델비 투약군 235명과 대조군 233명(에리불린, 비노렐빈, 카페시타빈, 젬시타빈 단일 요법)을 1대 1로 무작위 배정했으며 이전에 ▲항암화학요법을 받은 횟수(2회, 3회, 3회 초과) ▲뇌 전이 여부 ▲북미 또는 이외 지역으로 구분했다. 치료 전 최소 4주간 안정적인 뇌전이 상태를 보인 환자도 참여했으며 529명 중 61명에서 뇌 전이가 있었다. 평균 연령은 54세(27~82살)였다.
대조군 233명의 항암화학요법 단일군 배정 비중은 에리불린 54%, 비노렐빈 20%, 카페시타빈 13%, 젬시타빈 12% 순이었다. 앞서 환자들이 받은 치료를 보면 탁산 계열(100%), 안트라사이클린 계열(82%), 카보플라틴(66%), PD-1 또는 PD-L1(27%), PARP 억제제(7%) 등이었다.
트로델비군은 임상 21일 주기의 1일과 8일에 10mg을 정맥 주사했다. 대조군에서는 에리불린을 투약 21일 주기 중 1일과 8일에 정맥 주사로, 비노렐빈은 매주 1일 정맥 주사, 카페시타빈은 21일 주기의 1일부터 14일까지 하루 두 번 경구 투여했다. 젬시타빈28일 주기의 1일, 8일, 15일에 정맥 주사했다.
임상은 질병 진행 또는 허용 불가한 독성 발생, 사망 등이 발생할 때까지 실시했으며 트로델비로 교차 투여는 허용하지 않았다. 연구에서 임상을 중단한 경우 대부분 질병 진행(78%)이었고 부작용은 3%였다.
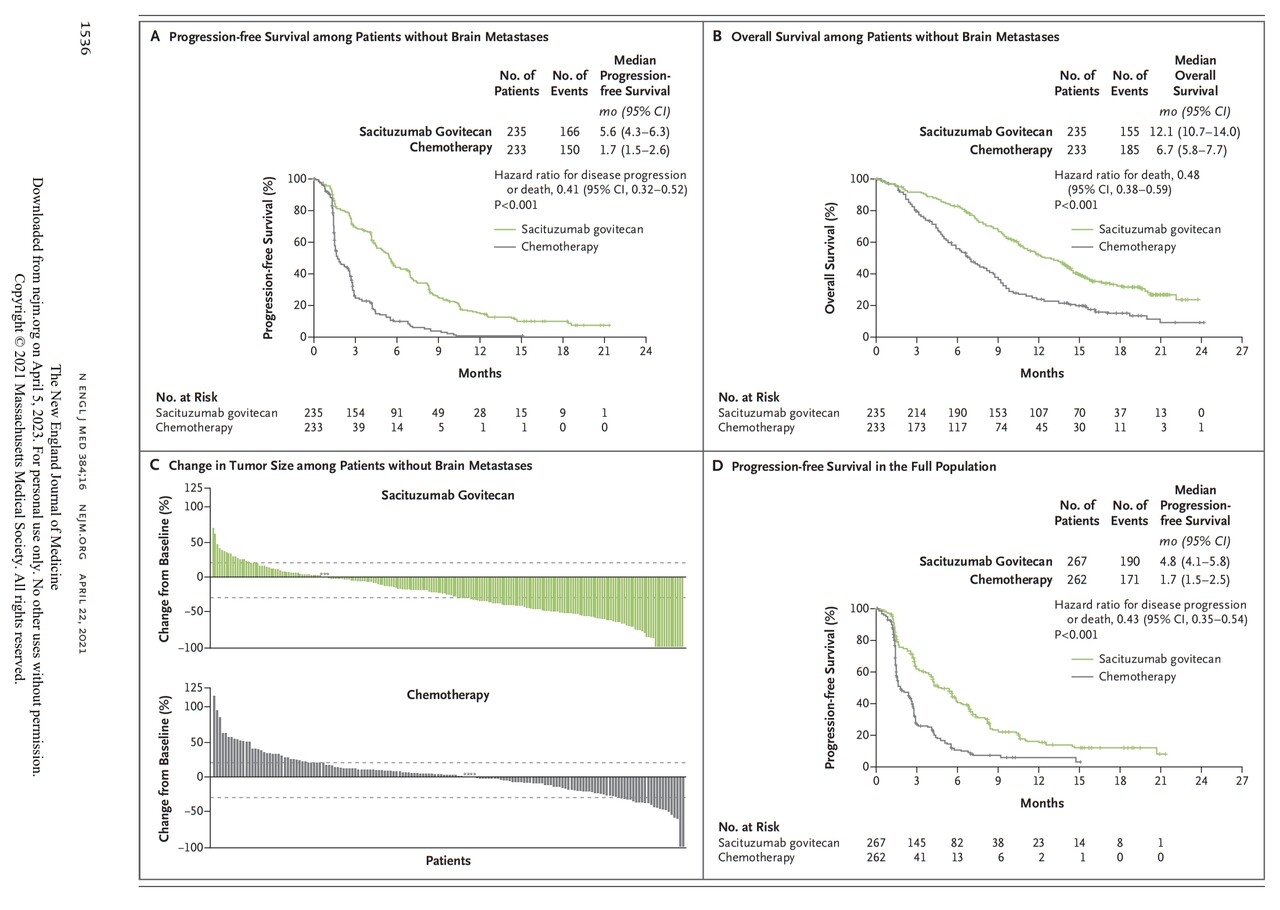
임상 1차 평가변수는 맹검독립평가위원회(Blinded Independent Review Committee, BIRC)가 분석한 뇌전이가 없는 환자들에서 무진행 생존기간이었다. 임상은 추적관찰기간 중앙값 17.7개월 시점에 중단 권고가 내려졌다. 트로델비 무진행 생존기간은 5.6개월, 대조군 1.7개월로 효과를 입증했기 때문이다.
연구자 평가에 따른 무진행 생존기간은 트로델비 5.5개월, 대조군 1.7개월로 동일했으며 전체생존기간 중앙값은 각각 12.1개월과 6.7개월로 두 배 이상의 차이가 났다.
▶뇌전이 상관없이 다양한 하위 분석 통해 생존기간 입증
트로델비가 좋은 평가를 받는 것은 다양한 상태를 가진 환자에서 생존기간 개선 효과를 보였기 때문이다.
전체 환자 529명에 대한 트로델비와 대조군 투약 결과 객관적 반응률은 35%대 5%로 차이가 있었고 뇌전이 여부와 상관없이 트로델비 투약군의 전체생존기간 중앙값은 11.8개월로 1년에 가까웠지만 대조군은 6.9개월로 차이가 있었다. 반응지속기간 중앙값(mDoR) 또한 6.3개월대 3.6개월로 임상적 혜택이 확인됐다. 반응을 보이기까지 걸린 시간은 두 군 모두 1.5개월로 비슷했다.
뇌 전이가 없는 환자 468명의 하위 분석을 보면 ▲65세 이상 환자에서 무진행 생존기간 중앙값 트로델비군 7.1개월 대비 2.4개월 ▲3회 이상 치료받은 환자에서 5.6개월대 2.5개월 ▲PD-1 또는 PD-L1 억제제 투여 환자에서 4.2개월대 1.6개월 ▲초기 진단 시 TNBC 환자 4.2개월대 1.5개월 ▲TNBC가 아니었던 환자 5.7개월 1.6개월 ▲간 전이 환자 4.2개월대 1.5개월로 모두 통계적으로 유의했다.
부작용은 트로델비 투약군, 대조군 모두 발생했다. 심각한 부작용은 트로델비 39명(15%), 대조군 19명(8%)이었고 치료 중단은 모두 12명(5%)이 발생했다. 사망자는 트로델비 투약군에서 호흡 부전(2명), 폐쇄성 폐렴(1명)이 있었으나 치료 관련성은 인정되지 않았다.
관련기사
개의 댓글
댓글 정렬
그래도 삭제하시겠습니까?

