[팜뉴스=이권구 기자] 소프트웨어 의료기기 임상시험 승인 건수가 최근 5년 간 지속적으로 증가했다. 또 지난해 디지털 치료기 임상시험계획 승인 건수가 전년대비 2배 이상 늘었다.
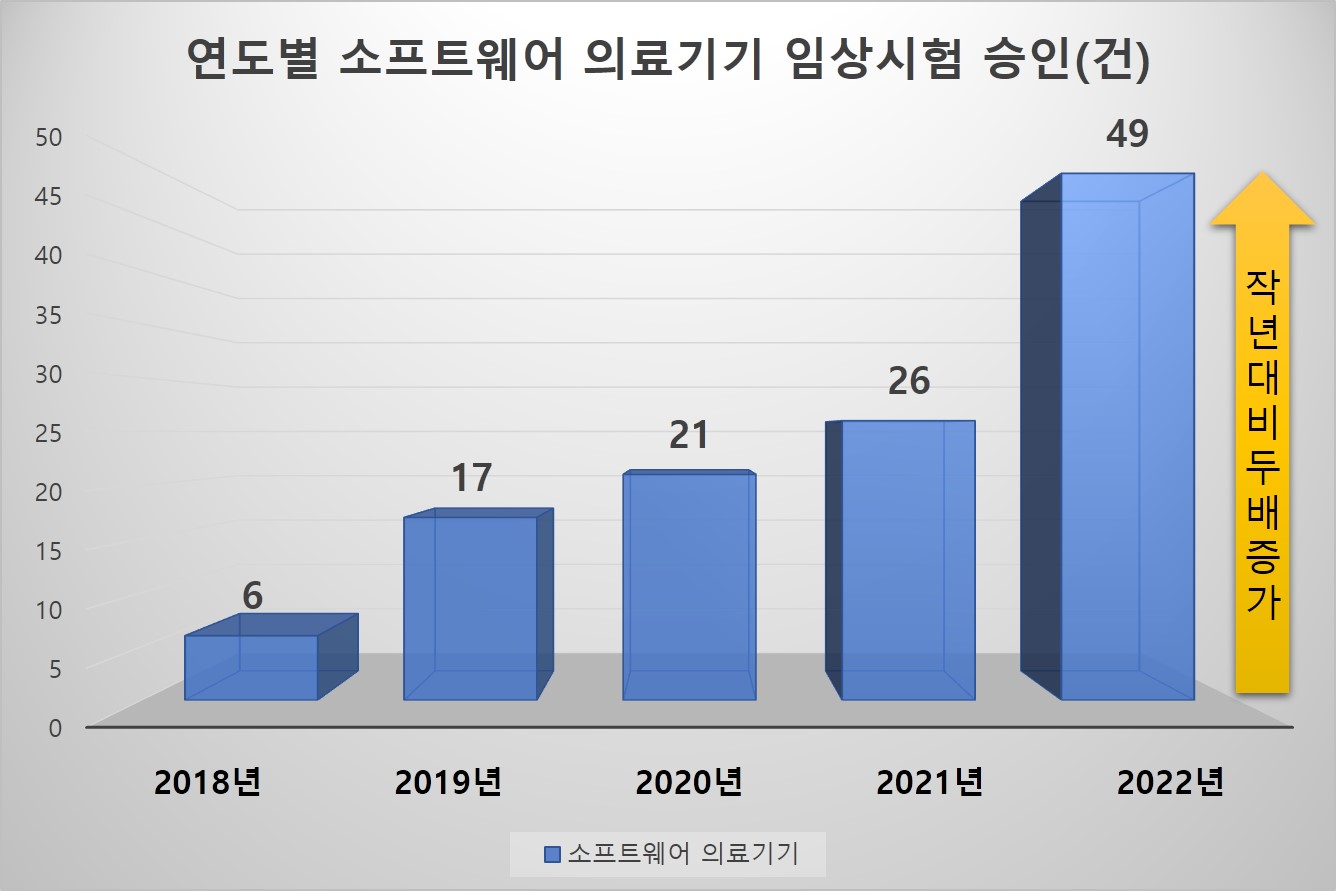
식품의약품안전처가 13일 낸 ' 2022년 소프트웨어 임상시험계획 승인 및 분야별 승인 제품 현황'에 따르면 소프트웨어 의료기기 임상시험계획 승인 건수는 지난 5년 간 꾸준히 상승해 2018년 6건 대비 지난해 49건으로 큰 폭으로 증가했다.
< 소프트웨어 의료기기 임상시험 승인 건수 현황(연도별) >
분야별 승인 건수는 ▲인공지능(AI) 기반 소프트웨어 등 진단 보조·예측(31건) ▲디지털 치료(보조)기기 등 치료·완화(17건) ▲증강현실(AR) 기반 수술 보조 소프트웨어 등 수출·치료·보조(1건) 순으로 ‘진단 보조·예측’ 분야 제품이 다수를 차지했다.
디지털 치료(보조)기기 분야에서는 2021년 9건의 임상시험계획이 8개 질환에 대해 승인됐으나, 지난해 17건의 임상시험계획이 12개 질환에 대해 승인됐다.
< 디지털 치료(보조)기기 임상시험 적용 질환 현황 >
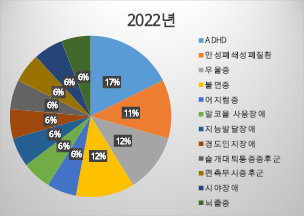
그간 디지털 치료(보조)기기는 불면증이나 중독증상 완화를 위한 제품 개발이 주류였던 것과 비교해 지난해에는 ADHD, 경도인지장애, 발달장애 등 보다 다양한 질환에 적용이 시도되고 있는 것이 확인됐다.
한편 지난해 승인된 49건 중 개발 초기 단계 탐색 임상시험(소수 임상시험 대상자로 비교적 단기간 실시되는 초기 임상시험)은 16건이었으나 허가를 위한 확증 임상시험(통계적으로 유의한 수 임상시험 대상자 대상 임상시험)이 33건으로 더 많았다.
소프트웨어 의료기기=소프트웨어만으로 개발·제조돼 허가·인증·신고한 의료기기로 크게 ▲질병 ‘진단 보조·예측’ ▲질환·증상 ‘치료·완화’(최근 ‘디지털 치료(보조)기기’로 불림) ▲‘수술 치료·보조’ 분야로 나뉨
개의 댓글
댓글 정렬
그래도 삭제하시겠습니까?

