[팜뉴스=김응민 기자] 최근 큐라클이 개발 중인 경구용 망막혈관질환 후보물질 'CU06'에 대한 임상 2a상 결과를 놓고 업계의 이목이 쏠리고 있다. 임상시험에서 확인하고자 하는 주요 연구결과인 1차 평가지표에 대해 다양한 의견이 제시되고 있기 때문이다.
일각에서는 통계적 유의성이 확보되지 않았다는 의견이 나오고 있지만 전문가들은 망막혈관질환 치료제 시장의 상황과 맥락을 이해해야 한다는 목소리다. 기존에는 없었던 새로운 기전의 약물(First-in-class)인 까닭에 임상 2상을 a상과 b상으로 나누어 진행하며 각각의 연구에서 추구하는 목적에 주목해야 한다는 것이다.

난치성 혈관질환 신약개발 전문기업 큐라클은 최근 공시를 통해 경구용 당뇨병성 황반부종(DME, Diabetic Macula Edema) 치료제 'CU06'의 미국 임상 2a상 톱라인 결과를 발표했다.
당뇨병성 황반부종 환자 67명을 대상으로 진행된 임상 2a상은 총 12주에 걸쳐 CU06 치료제를 100, 200, 300mg을 1일 1회 경구 투여한 후 나타나는 변화를 관찰했다.
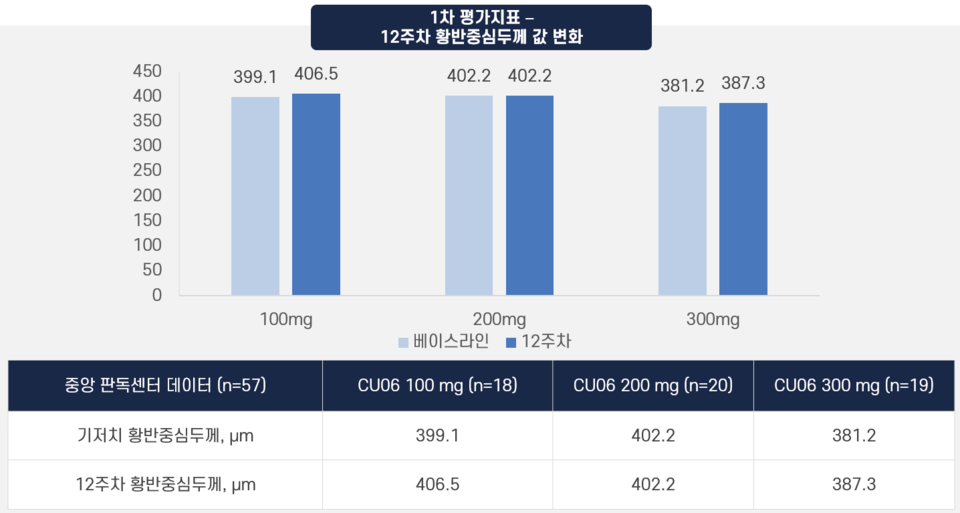
1차 평가지표는 시작점 대비 12주차에 부종의 두께가 얼마나 변화했는지를 보는 황반중심두께(CST) 변화 값을 측정하는 것이었고, 2차 평가지표는 시력개선 효과를 확인하기 위한 베이스라인 대비 12주차에서의 최대교정시력(BCVA) 점수 변화였다.
황반중심두께(CST, Central Subfield Thickness)란 망막에서 눈의 중심 시력을 담당하는 황반 중심 부분의 두께를 의미한다. 황반에 체액이 축적돼 발생한 부종의 두께는 정량적으로 평가하는 방식으로 측정된다.
최대교정시력(BCVA, Best Corrected Visual Acuity)은 안경 및 렌즈와 같은 시력 교정 도구를 사용해 측정한 '최상의 교정된 시력'을 뜻한다. 약물의 시력개선 효과 측정을 위해 규제당국에서 확인하는 주요 지표로 BCVA 70점은 시력검사 차트에서 70글자를 읽을 수 있는 수준이다(통상적인 시력 0.5).
총 3개월간의 임상시험 결과, 부종의 추가적인 진행은 관찰되지 않았으며 3가지 용량 모두에서 시력개선 효과가 확인됐다.
논란이 일어났던 대목은 바로 하위그룹 분석에 대한 내용이었다.
임상시험 결과에서 언급된 '환자군 간의 통계적으로 유의미한 결과가 베이스라인 대비 12주차에 CST 변화에 대한 1차 유효성 평가지표에서 관찰되지 않았다'라는 문구가 '1차 평가지표'를 달성하지 못했다는 오해를 불러일으킨 것.
하지만 여기에는 '숨은 일 인치'가 있다. 앞서의 내용은 100mg 투약군이 부종의 악화를 중단한 정도와 200mg 군이 악화를 중단한 정도, 그리고 300mg 군이 악화를 중단한 정도에서 '통계적인 차이'가 있는지에 대한 의미이다.
즉, '통계적으로 유의미한 결과가 관찰되지 않았다'라는 것은 3가지 용량군이 부종의 악화를 중단한 정도가 같기 때문에 '차이가 없다'라는 것이며, 모든 투약군에서 부종의 악화를 중단시켰다는 설명이다.
큐라클 관계자는 "하위그룹은 과거에 안구 내 주사제(Anti-VEGF)로 치료를 했던 그룹과 치료하지 않은 그룹, 부종 두께가 두꺼운 그룹과 얇은 그룹을 뜻한다"라고 밝혔다.
이어 "CU06은 부종의 유무 및 주사제 사용의 유무와 상관없이 모든 그룹에서 동일하게 부종의 악화를 중단했으며 그 정도가 통계적 차이가 없이 똑같은 것으로 해석해야 한다"라고 덧붙였다.
이뿐만이 아니다. 큐라클이 개발하는 경구용 당뇨병성 황반부종(DME, Diabetic Macula Edema) 치료제 'CU06'은 새로운 작용기전의 약물(first-in-class)로 개발되는 까닭에 임상시험 단계에서부터 차이점이 존재한다는 것이다.
임상2상 시험은 환자군에서 치료적 유효성을 탐색해 적정 용량과 투여기간을 설정하기 위한 정보수집을 목적으로 진행되는 임상시험이다.
기존에 시판되는 치료제가 있거나 작용기전이 알려진 약물은 보통 임상2상을 나누지 않고 한 번에 진행한다. 기존 연구에서 확보된 데이터를 통해 해당 약물이 임상에서 어떤 효과와 안전성을 보일 것인지 어느 정도 예측이 가능하기 때문이다.

반면, 큐라클은 CU06 당뇨병성 황반부종 임상2상을 2a상과 2b상으로 나눠서 연구를 진행하고 있다.
세계 최초의 혈관내피기능장애 차단제로 개발되고 있는 CU06처럼 새로운 작용기전을 가진 약물은 사람에게서 효과와 안전성을 보일 것인지, 어떤 환자군에 작용하고 적정용량이 어느 정도인지 등에 대한 약물의 사전 정보가 거의 없다.
따라서 어느 정도 규모가 있는 임상2상을 진행하기 위해서는 불확실성과 위험성을 줄일 필요가 있으며 '탐색적 목적'의 소규모 임상 2a상을 먼저 실시한다. 이후 2a상에서 얻은 효과와 안전성에 대한 사전 정보를 바탕으로 임상 2b상을 진행하게 되는 것이다.
임상개발 전문가는 "2a상에서의 성공·실패 기준은 치료제로서의 개발 가능성과 후속 임상을 진행할 수 있는 충분한 근거 확보 여부"라며 "이번 큐라클의 발표를 살펴보면 후기 임상의 설계에 필요한 정보를 확인하는 목적이 충분히 달성된 것으로 보인다"라고 전했다.
이어 "특히 망막혈관 치료제 승인에 요구되는 최종 평가지표인 최대교정시력에서 개선을 확인한 점은 후기 임상 진입 후 성공 가능성이 매우 긍정적일 수 있다는 것을 시사한다"라고 덧붙였다.
관련기사
개의 댓글
댓글 정렬
그래도 삭제하시겠습니까?

