[팜뉴스=김민건 기자] 한국릴리(대표 크리스토퍼 제이 스톡스) RET(REarranged during Transfection) 표적 치료제 '레테브모(셀퍼카티닙)'가 14일 국내 출시됐다.
레테브모는 융합 및 점 돌연변이를 포함한 RET 유전자 변이를 표적하는 기전이다. 지난 3월 RET 표적 치료제 중 처음으로 식품의약품안전처 허가를 받았다. 허가 적응증은 ▲전이성 RET 융합-양성 비소세포폐암 성인 환자 ▲전신요법을 요하는 진행성 또는 전이성 RET변이 갑상선 수질암이 있는 성인 및 만 12세 이상 소아 환자 ▲방사선 요오드에 불응하고, 이전 소라페닙 또는 렌바티닙 치료 경험이 있으며 전신요법을 요하는 진행성 또는 전이성 RET 융합-양성 갑상선암 성인 환자다.
크리스토퍼 제이 스톡스 한국릴리 대표는 "항암치료 패러다임이 바이오마커에 기반해 적합한 항암제를 투여하는 방향으로 빠르게 발전하고 있다. 레테브모는 RET 유전자 돌연변이를 표적하는 최초의 허가 받은 치료제로 RET 유전자 돌연변이 암 환자들이 자신에게 적합한 치료를 받을 수 있도록 레테브모 임상적 혜택을 국내 임상 현장에 적극 알릴 것"이라고 말했다.
▶허가 근거 임상 LIBRETTO-00
레테브모 허가 근거 임상은 RET 유전자 변이 환자를 대상으로 한 1/2상 'LIBRETTO-001'다. 해당 연구는 이전에 치료를 받은 경험이 있거나 없는 RET 융합-양성 비소세포폐암 환자, RET-변이 갑상선 수질암 환자, RET 융합-양성 갑상선암 환자 등 총 702명이 참여했다.
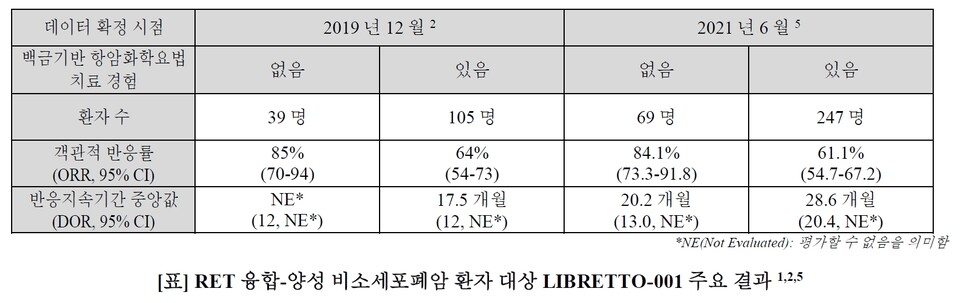
이 연구에서 레테브모는 RET 융합-양성 비소세포폐암 환자군을 대상으로 ▲이전에 백금기반 항암화학요법 치료 경험이 없는 경우 객관적 반응률(Overall Response Rate, ORR) 85%(95% CI, 70-94)을 확인했고 ▲백금기반 항암화학요법 치료 경험이 있는 경우 ORR은 64%(95% CI, 54-73), 반응지속기간(Duration of Response, DoR) 중앙값은 17.5개월(95% CI, 12.0-NE)을 보였다.
올해 4월 유럽종양학회 폐암 학술대회(European Lung Cancer Congress, ELCC)에서 발표된 LIBRETTO-001 추가 분석에서는 지속적인 유효성을 보였다. 레테브모를 RET 융합-양성 비소세포폐암 환자 중 ▲백금기반 항암화학요법 치료 경험이 없는 환자에서 사용 시 ORR 84.1%(95% CI, 73.3-91.8), mDoR 20.2개월(95% CI, 13.0-NE) ▲백금기반 항암화학요법 치료 경험이 있는 환자에서 ORR 61.1%(95% CI, 54.7-67.2), mDoR 28.6개월(95% CI, 20.4-NE)을 보였다.
▶중추신경계서 확인한 객관적 반응률
뇌전이 비소세포폐암 환자에 대한 레테브모 임상 데이터도 업데이트됐다. 레테브모는 기존 연구 논문에서 백금 기반 항암화학요법 치료 경험이 있고 뇌전이 부위 측정이 가능한 RET 융합-양성 비소세포폐암 환자 11명 중 10명에서 중추신경계 객관적 반응을 확인했다.
릴리는 이번에 새로 발표된 레테브모 중추신경계(Central Nervous System, CNS) ORR이 84.6%(95% CI, 65.1-95.6)로 확인됐고, 특히 완전반응(Complete Response, CR)을 보인 환자는 26.9%였다고 밝혔다. 아울러 레테브모 치료 환자의 두개 내(Intracranial) 무진행생존기간(Progression-free survival, PFS) 중앙값은 19.4개월이라고 했다. 릴리는 RET 변이 4기 폐암 환자 46%, 즉 약 2명 중 1명은 일생동안 뇌전이를 경험한다고 한 연구 결과를 인용했다.
안진석 삼성서울병원 혈액종양내과 교수는 "폐암은 사망률이 가장 높은 암종으로 일반적으로 뇌전이 발생 시 예후가 좋지 않다. 특히 RET 변이가 있는 4기 폐암 환자의 뇌전이 발생률은 비소세포폐암 환자에서 확인된 뇌전이 발생률보다 두 배 이상 높지만 지금까지는 표적 치료 옵션의 부재로 일반 암 환자와 동일하게 항암화학요법을 진행할 수밖에 없었다"고 말했다. 안 교수는 "레테브모가 뇌전이 환자를 포함해 RET 유전자 돌연변이 암 환자를 대상으로 계속해서 의미 있는 임상적 근거를 보여주고 있는 만큼 이번 출시 이후 하루빨리 보다 많은 국내 환자들에게서 접근성이 개선됐으면 한다"고 말했다.
▶ RET 변이에 의한 갑상선암 환자들에게 새로운 치료 기회 제공
릴리는 레테브모가 RET변이 갑상선 수질암과 RET 융합-양성 갑상선암 환자군에서도 유효성과 안전성을 보였다고 밝혔다. 이전에 반데타닙 또는 카보잔티닙 치료 경험이 없는 RET변이 갑상선 수질암 환자군에서 레테브모 ORR은 73%(95% CI, 62-82), mDoR 22.0개월(95% CI, NE-NE)로 나타났다. 반데타닙 또는 카보잔티닙 치료 경험이 있는 환자군에서는 ORR 69%(95% CI, 55-81)였고, 추적기간 DoR은 중앙값에 도달하지 않았다는 것이다.
아울러 릴리는 이전에 소라페닙 또는 렌바티닙 치료 경험이 있는 RET 융합-양성 갑상선암 환자군에서 레테브모 ORR 79%(95% CI, 54-94), mDoR 중앙값은 18.4개월(95% CI, 7.6-NE)로 확인했다고 설명했다.
이 경우 이상반응은 일반적인 경우 아스파르테이트 아미노전이효소(aspartate aminotransferase, AST)와 알라닌 아미노전이효소(alanine aminotransferase, ALT) 증가, 포도당 증가, 백혈구 감소, 혈액 내 알부민 감소, 혈액 내 칼슘 감소, 입 건조, 설사, 크레아티닌 증가, 고혈압 등이었다. 이는 지난 4월 발표한 추가 분석에서도 일관된 이상반응이 나타났다.
키워드
#레테브모관련기사
개의 댓글
댓글 정렬
그래도 삭제하시겠습니까?

