
[팜뉴스=김민건 기자] 크론병·궤양성대장염 치료제 킨텔레스(베돌리주맙)가 피하주사 제형으로 되돌아왔다. 정맥주사와 동일 환자군에 피하주사 치료 옵션을 제공하면서 투여 편의성을 개선했다.
17일 한국다케다제약(대표 문희석)은 식품의약품안전처로부터 킨텔레스 프리필드펜주 시판 허가를 받았다고 밝혔다.
킨텔레스는 항인테그린제제 중 크론병과 궤양성대장염 치료에 사용가능한 유일한 치료제다. 그간 병원을 방문해 투여하는 정맥주사(Intravenous injection, IV) 제형으로 사용 가능했다. 킨텔레스 정맥주사 1회 투여 시간은 30분이다. 이에 더해 피하주사제(Subcutaneous injection, SC) 추가 허가를 받아 환자 스스로 투여할 수 있게 됐다.
킨텔레스 피하주사제는 정맥주사와 동일한 적증응을 가진다. 중증도에서 중증의 활성 크론병 또는 궤양성대장염 치료가 목적이다. 투여 방법은 킨텔레스주300mg을 0주차 또는 2주차에 정맥 주입 후 6주차 시점에 반응을 보이는 환자에게 그 이후 매 2주마다 108mg을 피하 주입하면 된다.
킨텔레스 피하주사는 해외에서 먼저 승인받아 사용 중이다. 지난 2020년부터 유럽, 캐나다, 오스트레일리아 등 주요 시장에진출해 있다.
김태훈 한국다케다제약 소화기사업부 총괄은 "염증성장질환은 젊은 나이에 발병해 증상이 만성적으로 지속되는 질환이기 때문에 꾸준한 관리를 위한 치료 순응도가 무엇보다 중요하다"고 말했다.
그는 "많은 염증성장질환 치료제가 단일 제형인 점을 감안할 때, 장에만 작용하는 킨텔레스의 치료 옵션을 정맥주사나 피하주사 모두 제공하면서 치료 편의성을 개선할 수 있게 됐다"고 말했다.
▶킨틸레스 피하주사 효과와 안전성
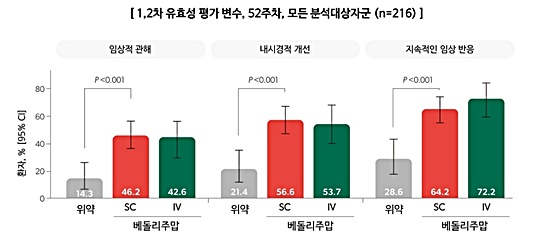
킨텔레스 피하주사는 'VISIBLE 1' 임상연구를 통해 성인 궤양성대장염 환자의 유지 치료에 대한 효과와 안전성 프로파일을 확인했다.
VISIBLE 1은 3상, 무작위 배정, 플라시보 대조, 이중맹검, 이중위약 연구다. 29개국 141개 기관의 중등도-중증 성인 궤양성대장염 환자를 대상으로 시행됐다.
대상 환자 216명을 분석한 결과, 피하주사는 이전에 항TNF 치료 경험과 관계없이 위약군 대비 정맥주사와 일치하는 유의한 효과를 보였다.
아울러 안전성 프로파일(주사 부위 반응 제외), PK 노출, 면역원성을 보였다. 환자 평가 결과는 유효성, 안전성, 내약성 결과와 일치하며 개선을 보였다. 환자 삶의 질에 효과를 확인했다.
▶크론병에서 치료 유지 효과
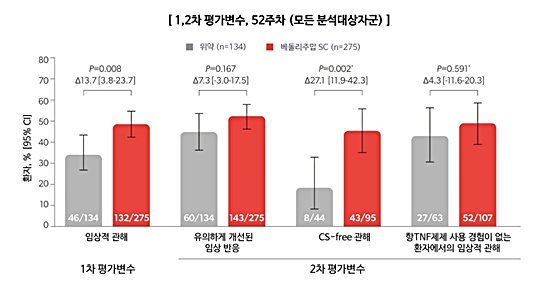
VISIBLE 2 임상 연구에서는 성인 크론병 환자의 유지 치료로 킨텔레스 피하주사를 평가했다.
VISIBLE 2는 3상, 무작위 배정, 플라시보 대조, 이중맹검 연구로, 30개국 169개 기관의 중등도-중증 성인 크론병 환자를 대상으로 시행됐다.
연구에 참여한 410명을 분석한 결과, 1차 평가변수인 52주차에서 임상적 관해를 킨텔레스 피하주사 유지 치료군의 48.0%가 달성했다. 위약군은 34.3%였다. 피하주사 유지 치료군과 위약군 간 전체 안전성 결과는 유사했다.
개의 댓글
댓글 정렬
그래도 삭제하시겠습니까?

