
비소세포폐암 항암제인 타그리소(오시머티닙)의 심장독성 문제가 수면 위로 떠올랐다. 지난 2018년부터 심장독성에 대한 연구가 꾸준히 발표된 데 이어, 이번에는 미국심장학회지에 다시 한번 해당 부작용에 대한 연구결과가 올라왔기 때문이다.
타그리소는 특정 암세포와 일부 정상 세포의 표면에 있는 EGFR(상피세포 증식 인자)을 표적으로 해 종양 세포의 성장을 차단하도록 고안된 3세대 항암제다. 주로 EGFR-TKI에 내성이 있는 환자에게 1‧2세대 치료제로 활용된다.
특히 지난 2017년부터 건강보험 급여권에 들어오면서 국내 처방 규모가 크게 증가했다. 업계에 따르면, 올해 2월까지 타그리소의 원외 처방액은 158억원을 기록 중이다. 이는 작년 동기대비 약 26% 증가한 수치다.
하지만 최근 몇 년간 안전성에 대한 지적이 끊이질 않고 있다. 바로 ‘심장독성’에 대한 내용이다.
2018년에 세계적인 의학저널 ‘뉴잉글랜드 저널 오브 메디슨(NEJM)’을 통해 게재된 논문에 따르면, FLAURA 연구에서 타그리소는 대조군 대비 심장 부작용을 유발하는 심전도 QT 연장시간(ECG QT prolongation)이 2배 이상 높았다. 타그리소 투여군에서 발생한 심장 부작용 환자 수는 28명(10%)이었던 데 반해 대조군은 11명(4%)으로 확인됐다.
심부전에 대한 발생률도 타그리소가 더 높았다. 심부전(cardiac failure)은 타그리소에서 12명(4%)이, 대조군인 표준 EGFR-TKI에서는 6명(2%)이 발생했다. 또한 CTCAE(이상반응 평가도구) 3등급 이상의 심장 부작용이 보고된 비율 역시 타그리소 2.2%, 대조군 0.7%로 타그리소가 더 높은 것으로 보고됐다.
이뿐만이 아니다. 지난해 미국임상종양학회 연례학술대회에서도 같은 문제점을 지적한 것.
학술대회에서 발표한 FDA 이상반응보고시스템(FAERS, FDA adverse events reporting system)에 따르면 타그리소 치료 환자 중 이상 반응이 나타난 2,454명 중에서 150명이 심장독성과 관련이 있는 것으로 밝혀졌다.
이들의 중위연령(median age) 범위는 64세에서 79세였고 환자 대다수는 상태가 심각해 병원에 입원하거나 사망한 것으로 알려졌다.
주목할 점은 이번에 일본 연구진이 미국심장학회지(JACC)에 발표한 자료가 리얼월드데이터(RWD, real world data)를 기반으로 작성됐다는 것.
RWD는 환자들이 실제로 처방받은 의약품 자료를 바탕으로 만들어지는 만큼 활용 가능성이 높은 것으로 평가받고 있다. 때문에 선진국을 중심으로 RWD와 관련된 의약품의 재심사나 적응증 추가확대, 신규 허가 등과 같은 다양한 시범사업이 진행되고 있다.
일본 오사카의 국제암센터 연구진은 ‘오시머티닙(타그리소)으로 치료받은 EGFR 변이 비소세포폐암 환자의 심장 부작용’이란 연구 보고서를 3월자 JACC: CardioOncology에 발표했다(doi.org/10.1016/j.jaccao.2020.02.003).
연구진은 2014년부터 2019년까지 오사카의 국제암센터에서 타그리소로 치료받은 환자 중에서 EGFR 변이가 발생한 비소세포폐암 환자 123명에 대한 자료를 분석했다.
그 결과, 아래 표와 같이 전체의 4.9%에 해당하는 6명의 환자에서 CTCAE 3단계 이상의 심각한 심장 부작용이 관찰됐다. 심장 부작용 증상은 ▲심부전증(3명) ▲심장판막증(2명) ▲급성심근경색(1명)으로 확인됐다.
[표. 오시머티닙(타그리소)로 인해 발생한 심장 부작용 사례]
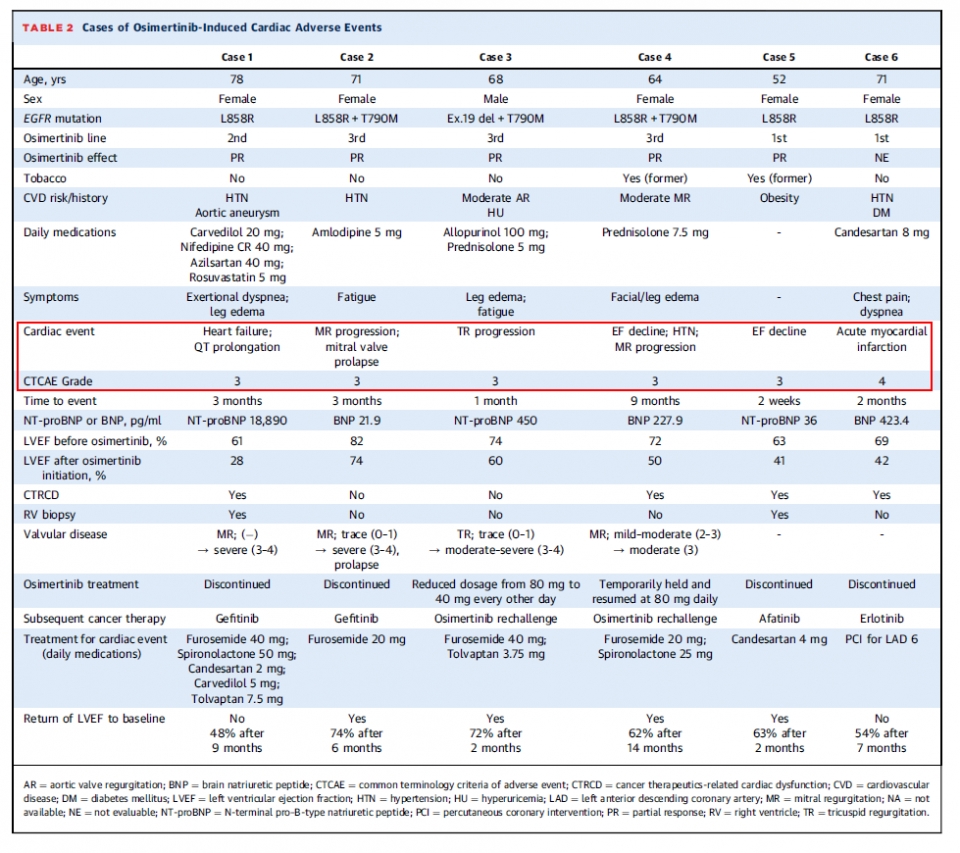
CTCAE(Common Terminology Criteria for Adverse Events)는 미국국립암연구소가 개발한 분류기준으로 암 치료에 사용하는 약물의 부작용을 보고할 때 사용하는 양식이다. 이번 연구에서는 CTCAE 5.0 버전을 적용했다.
연구진은 “타그리소로 치료받은 환자의 심장 부작용 발생률은 임상시험에서 관찰된 수치와 유사하지만 일본에서 시판 후 조사한 수치보다 높았다”며 “비소세포폐암 치료에 있어 타그리소는 핵심적인 치료제인 만큼 추가적인 연구를 통해 심장 부작용을 관리하는 것이 중요하다”고 밝혔다.
개의 댓글
댓글 정렬
그래도 삭제하시겠습니까?

