[팜뉴스=김민건 기자] 1인 맞춤형 치료제이자 1회 치료로 끝나는 원샷 치료제. 세계 최초 맞춤형 항암제 '킴리아(Kymriah, 티사젠렉류셀)'를 국내에서도 정식 사용할 수 있게 됐다. 킴리아는 작년 8월부터 시행된 첨단재생바이오의약품 1호 치료제라는 상징성도 획득했다.
한국노바티스(대표 조쉬 베누고팔)는 5일 식품의약품안전처로부터 킴리아 허가를 받았다고 밝혔다.
허가 적응증은 ▲25세 이하의 소아 및 젊은 성인 환자에서 이식 후 재발 또는 2차 재발 및 이후의 재발 또는 불응성 B세포 급성 림프성 백혈병(ALL)의 치료 ▲두 가지 이상의 전신 치료 후 재발성 또는 불응성 미만성 거대 B세포 림프종(DLBCL) 성인 환자의 치료이다.
킴리아는 '바이오의약품 품질·안전 관리 강화 및 지원' 등을 위해 작년 8월부터 시행된 첨단재생바이오법(이하 첨바법) 의 1호 치료제가 됐다.
식약처는 "첨단재생바이오법 심사 기준에 따라 품질, 안전성·효과성, 시판 후 안전관리계획 등을 과학적으로 철저하게 심사·평가했다"며 "첨단재생바이오법 제30조에 따른 '장기추적조사' 대상"이라고 설명했다. 이에 따라 투여일로부터 15년간 이상사례 현황을, 최초 판매한 날로부터 1년 마다 장기추적조사 결과를 식약처에 보고해야 한다.
◆기존 치료제와 다른 1인 맞춤형, 제조·보관도 특별
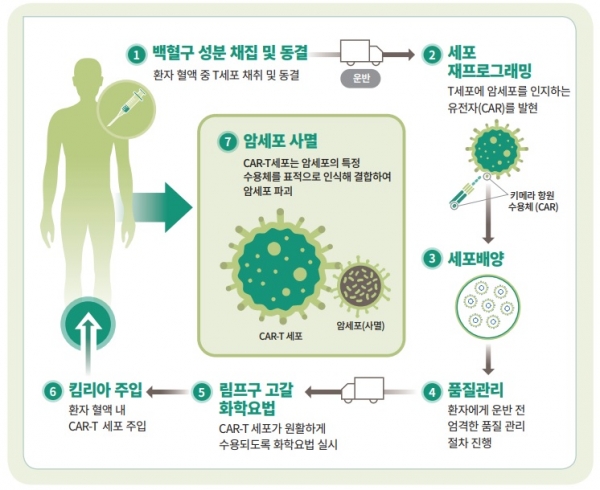
CAR-T 치료제는 환자에서 채취한 T세포 표면에 암세포의 특정 항원을 인지하는 키메릭 항원 수용체(Chimeric Antigen Receptor, CAR)가 발현될 수 있도록 유전적으로 재조합시킨 후 다시 환자의 몸에 주입하는 방식이다.
이에 킴리아는 CAR를 코딩하는 외래도입유전자(transgene)를 환자 본인 T세포에 도입해 CD19 발현 세포를 구분 제거하도록 유전적으로 변형된 자가 면역세포 항암제로 개발됐다.
노바티스는 "세포∙유전자∙면역치료제 특성을 모두 갖춘 항암제로 단 1회 치료로 다른 치료 옵션이 없는 말기 혈액암 환자들을 완전 관해에 이르게 하고, 지속적인 반응을 보인다"고 설명했다.
첨단바이오의약품인 킴리아는 ▲세포 채취 ▲냉동 보존 및 운반 ▲개인 맞춤형 CAR-T 세포 제조 ▲환자에게 다시 주입하는 등 과정을 거쳐 만들어진다. 기존 의약품과 달리 고도화된 1인 맞춤형 공정 과정을 거치기 때문이다.
노바티스는 "킴리아는 각 도입 국가별로 전문 인력과 의료기관 훈련 및 인증 등으로 확보된 안전한 시스템, 제조 공장의 전문화된 과정을 통해 1인 환자 맞춤형으로 생산된다"고 강조했다.
◆킴리아, JULIET·ELIANA 연구 결과 근거로 허가
DLBCL과 ALL은 대부분 표준 항암화학요법으로 치료된다. 일부 소수 환자는 치료에 반응이 없거나 재발을 경험한다. 재발성∙불응성 환자들 중 조혈모세포 이식 등 2차 치료에도 실패한 경우 기대 여명이 약 6개월에 불과하다.
킴리아는 더 이상 치료 옵션이 없는 재발성∙불응성 DLBCL과 pALL 환자에게 장기 생존은 물론 일상 복귀까지 기대할 수 있는 새로운 항암제로 기대되고 있다.
식약처는 노바티스가 펜실베니아대학과 공동으로 진행한 임상 2상 연구인 JULIET과 ELIANA 연구 결과를 근거로 킴리아를 허가했다.
JULIET은 성인 재발성∙불응성 DLBCL 환자를 대상으로 한 연구다. 투여 3개월 만에 전체 반응률(Overall Response Rate, ORR)은 53%(NE, 95% CI, 10.02 - NE)였다. 완전 관해(Complete Remission, CR)는 39.1%(NE, 95% CI, NE)였다. 투여 2년 시점에서 무진행 생존율(progression-free survival, PFS)은 33%였다.
ELIANA는 소아 재발성∙불응성 ALL 환자를 대상으로 한 연구다. 연구 결과 투여 3개월 이내에 환자의 82%(95% CI, 72% - 90%)가 CR 또는 불완전 혈액 수치 회복을 보이는 완전 관해(Complete Remission with incomplete blood count recovery, CRi)를 달성했다.
관해에 도달한 환자 98%가 미세잔존질환(minimal residual disease, MRD)이 음성을 나타냈다. 6개월 시점에서 무사건 생존율(Event-free survival, EFS)은 73%(95% CI, 60% - 82%)였다.
노바티스는 "두 임상 연구 모두 임상적 유효성을 입증했으며 반응 지속 기간 중앙값(median Duration of Response, mDOR)과 전체 생존율 중앙값(median Overall Survival, mOS)에는 도달하지 않았다"며 "이는 반응을 보인 환자들이 킴리아 치료 후 효과가 지속되고 있다는 점을 반증한다"고 밝혔다.
윤성수 서울대병원 혈액종양내과 교수는 "킴리아는 그동안 항암제 역사상 없던 새로운 기전의 혁신적인 1인 맞춤형 치료제이자 1회 치료로 끝나는 원샷 치료제"라며 "이미 2번 이상의 치료와 이식에 실패해 기대 여명이 3~6개월에 불과한 재발성∙불응성 DLBCL 환자들에게 단 1회 치료로 완전 관해에 도달해 생존율을 높일 수 있다"고 말했다.
윤 교수는 "킴리아는 생존기간 향상뿐 아니라 1회 치료로 환자의 병원 방문을 줄여 환자와 다른 가족 구성원이 일상생활로 복귀할 수 있도록 돕는다는 점에서도 큰 의미가 있다"고 말했다.
유철주 연세대 세브란스병원 소아혈액종양과 교수도 "킴리아는 죽음을 목전에 두었던 어린 ALL 환자들에게 새 인생을 안겨줄 수 있는 기적의 치료제"라며 :처음 CAR-T 임상에 참여했던 미국의 소아 ALL 환자는 치료 후 현재까지 8년간 완전 관해 상태를 유지해 학교를 다니며 평범한 일상생활을 영위하고 있다"고 말했다.
2017년 8월 전세계 최초로 미국식품의약국(FDA) 허가를 받은 킴리아는 캐나다, 스위스, 일본, 호주, 독일 등 28개국에서 승인 받아 사용 중이다.
관련기사
개의 댓글
댓글 정렬
그래도 삭제하시겠습니까?

