식약처가 최근 의약품 품목허가·신고 갱신 관련 통계를 발표하면서 기준에 미달한 의약품 상당수를 정리했다고 홍보했다. 의약품품목허가갱신제에 따라 이룬 성과라는 의미였다. 하지만 전문가들 사이에서는 이번 통계가 제도의 ‘한계’를 여실히 보여줬다는 지적이 나오고 있다.
의약품품목허가갱신제는 품목허가·신고 이후에도 지속적인 안전성·유효성 확보와 효율적인 관리를 위해 5년마다 품목허가 또는 신고를 갱신하는 제도다. 제약사는 해당 품목의 허가증(또는 신고증)에 기재된 유효기간이 종료되는 날의 6개월 전까지 신청서를 작성해 제출해야 한다.
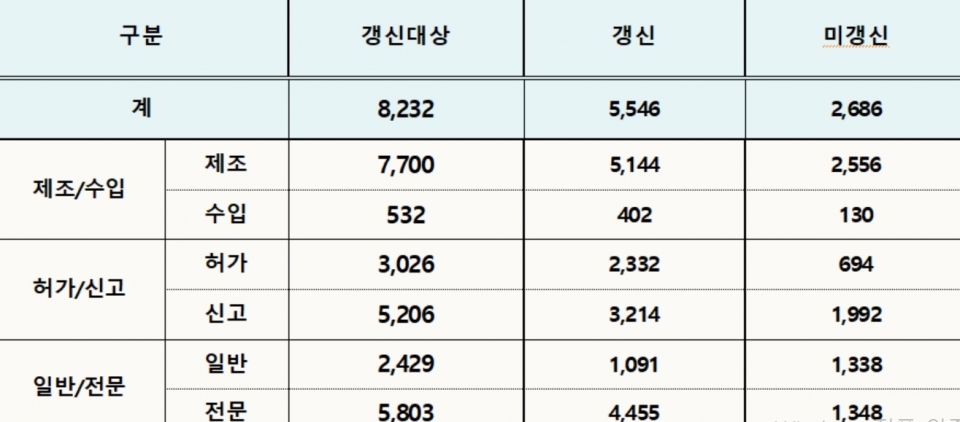
식약처는 지난 2년간(2017년 7월~2019년 6월) 의약품 품목허가·신고 갱신 현황을 분석한 결과, 전체 8,232개 중 67%인 5,546개 품목이 갱신됐다고 발표했다. 통계에 따르면 품목이 갱신된 5,546개 외에 나머지 2,686개 품목은 품목취하, 미신청 등 사유로 정리됐다. 이들 2,686개 품목 중 생산·수입실적이 없는 품목은 72%(1,938개)에 달했다.
식약처는 “허가는 받았으나 실제 생산실적이 없는 제품이 정비되는 등 의약품 허가 관리에 있어 갱신제도가 중요한 역할을 하고 있다”며 “의약품이 효율적으로 관리돼 국민들에게 안전과 품질이 확보된 의약품이 공급될 수 있도록 하겠다”고 밝혔다.
그런데 이번 통계엔 ‘숨은일인치’가 있다.
팜뉴스 취재 결과, 이번에 갱신에 실패한 2,686개 품목 중 28%가 품목을 자진 취하한 사례인 것으로 드러났다.
문제는 통계를 통해, 의약품품목허가신고갱신제의 ‘한계’가 여실히 드러났다는 점이다. 익명을 요구한 한 의사는 “제약사가 의약품을 생산하지 않거나(72%), 자료제출을 안하고 자진취하(28%)를 했다는 얘기다”며 “결국 갱신 제도를 통해 식약처가 적극적으로 퇴출한 약이 단 한건도 없다는 뜻”이라고 지적했다.
실제로 안전성과 유효성에 문제가 있는 의약품을 퇴출시킨다는 것이 이 제도의 기본 취지다. 제약사들이 품목갱신을 위해 안전관리에 관한 자료 및 조치계획, 외국 사용현황 및 안전성 조치 자료(의약품 관련 문헌집) 등의 갖가지 자료를 제출해야 하는 까닭이다.
이번 통계는 의약품품목허가신고갱신제가 단순한 의미의 ‘체크리스트’에 불과했다는 것을 여실이 보여줬다는 게 전문가들의 지적이다.
더구나 식약처는 과거 시행된 의약품 재평가를 대체하는 의미로 ‘수시평가’ 제도를 지난해 11월 도입했다. 당시 수시 평가의 요건 중 하나로 ‘품목허가(신고) 갱신 절차상 효능효과 등 입증이 미흡한 경우’를 명시했다.
앞서의 의사는 “의약품품목허가갱신제 통계를 보면 식약처가 내용 확인 없이 그야말로 자료를 냈는지만 확인한다는 점이 보인다”며 “과거 의약품 재평가 때는 중앙약심에서 의논하는 절차라도 있었다. 사실상 의약품 재평가 제도를 포기한 것과 다름없다”고 질타했다.
문제는 또 있다. 식약처 통계에 따르면, 전문의약품은 23%(1348개), 일반의약품 55%(1338개)가 품목 취소됐다. 의약품품목허가신고갱신제에 대한 제도적 보완이 필요하다는 지적이 들리는 까닭이다.
약업계 관계자는 “이렇게 많은 약들이 사라지는 것은 정상적인 상황이 아니다”며 “만약 해외에서 허가 받은 의약품들이 국내로 들어온 이후, 해당국의 의약품 문헌에서 허가 근거가 사라지면 심각한 문제가 생긴다. 이 경우 제약사에 책임을 물어야 하는데 자진취하를 하면 그만이다. 품목허가갱신제의 또 다른 빈틈”이라고 밝혔다.
품목허가신고갱신제 자체가 제약사들의 ‘쉬운 철수’를 방조하고 있는 만큼 품목 허가를 스스로 취하한 제약사들에 대한 ‘책임성 부과 방안’을 고민해야 한다는 뜻이다.
하지만 식약처의 입장은 다르다. 식약처 관계자는 “기본적으로 허가를 받았으면 안전성과 유효성이 확보된 것”이라며 “그 이후 허가를 유지하기 위해서 제약사가 허가받은 약품의 안전관리를 직접 수행하라는 것이 제도의 기본 취지다”라고 밝혔다.
그러면서 “생산 유통되지 않은 의약품을 정비했다는 것이 이번 통계의 핵심이다. 이점에 집중해야 한다”며 “의약품 안전성 평가는 갱신제 말고도 부작용 보고, RMP 등 다른 제도를 통해 꼼꼼히 이뤄지고 있다”고 해명했다.
개의 댓글
댓글 정렬
그래도 삭제하시겠습니까?

