[팜뉴스=김민건 기자] 첫 ALK 비소세포폐암(NSCLC) 치료제 잴코리 개발 이후 잠잠하던 화이자가 새로운 카드를 통해 분위기 반전을 노린다.
식품의약품안전처는 7월 29일 한국화이자 로비큐아정(롤라티닙, 미국명 로브레나)을 역형성 림프종 인산화효소(Anaplastic lymphoma kinase, ALK) 양성을 보이는 NSCLC 환자 2차 치료에 단독 사용을 허가했다.
로비큐아 투여 시 생존기간 개선을 입증한 자료는 없지만 반응률과 반응 기간에 근거한 유효성을 보고 허가했다.
이번 허가로 로비큐아는 국내에서 ALK 1차로 로슈 알레센자(알렉티닙)나 노바티스 자이카디아(세리티닙)를 사용했으나 병이 진행된 경우 사용할 수 있다. 또는 화이자 잴코리(크리조티닙) 등 최소 1개 이상의 다른 ALK 저해제로 치료했으나 증상이 진행된 경우에 투여할 수 있다.
로비큐아는 ALK와 C-ROS(ROS1) 유전 변이를 선택적으로 억제하는 키로키나신 저해제(TKI)이다. ALK 변이는 수용체에 EML4라는 단백질이 융합하는 과정에서 비정상적인 세포 증식 신호가 과다 발생해 암을 일으키게 된다.
현재 국내 ALK 표적치료제 시장에는 1세대 화이자 잴코리부터 2세대 노바티스 자이카디아와 로슈 알레센자, 다케다 알룬브릭(브리가티닙)이 경쟁 중이다. 화이자가 유일한 ALK 양성 NSCLC 1차 치료제로 잴코리를 선보일 때만 해도 500억원에 달하는 시장 매출액을 점유했다. 그러나 2세대 치료제가 1차 시장까지 확대하면서 점점 설자리를 잃어가고 있다.
ALK 양성 NSCLC 환자는 1차 치료 후 발생하는 내성과 중추신경계(CNS), 즉 뇌전이가 사망 위험을 매우 높인다. 환자의 60~90%는 두개 내(Intracranial) 전이를 겪는다. 잴코리는 복용 시 1년 내 내성이 발생한다는 치명적 약점을 가지고 있었다. 처음 ALK 양성 변이를 진단받은 환자 30~40%에서 잴코리 투여 시 재발 환자 70%가 뇌전이를 보인다. 잴코리 복용 환자에서 뇌전이가 발생하면서 2세대 ALK 표적치료제로 2차 치료를 해도 무진행생존기간(PFS) 중앙값은 1년 미만이다. 이에 미국종합암네트워크(NCCN, National Comprehensive Cancer Network) 가이드라인 등은 새로 개발되는 표적항암제를 ALK 1차 치료제로 권고하고 있다.
국내 한 대학병원 교수는 "ALK 변이 치료에서 중점적으로 고려하는 사항은 뇌전이 예방과 치료에 효과적이냐는 점"이라며 "뇌전이가 발생한 환자는 치료가 어려울 뿐만 삶의 질이 현저히 감소하면서 치료 를 유지하기 어렵다"고 말했다. 잴코리 이후 ALK 변이 표적항암제 개발 경향이 뇌전이 효과를 추구하게 되면서 화이자도 새로운 표적항암제 개발에 착수했고 이번에 로비큐아를 내놓았다.
시장에는 강력한 경쟁자가 있다. 올해 1차 급여 확대를 인정받은 다케다 알룬브릭이 내성 억제와 뇌전이에서 효과를 강점으로 시장을 공략하고 있다.
알룬브릭은 잴코리와 일대일로 비교한 임상 데이터를 가지고 있다. 특히 BIRC(맹검독립평가위원회) 평가에서 알룬브릭 PFS는 24개월로 잴코리 대비 2배 이상인 것으로 나타났다. ALK 양성 변이 1차 치료를 목적으로 한 연구자 평가에서도 PFS 29.4개월로 잴코리 대비 3배 이상의 효과를 확인했다. 알룬브릭 또한 뇌전이 환자의 두개내 mPFS가 24개월로 잴코리 대비 4배였고 두개내 반응지속기간(iDOR) 24개월, 두개내 객관적 반응률(iORR) 78%로 효과를 입증했다. 로슈 알레센자도 잴코리와 비교 임상을 통해 약 3배 이상 개선된 34.8개월의 mPFS 효과를 확인했다.
▶식약처가 평가한 3세대 ALK치료제 로비큐아
식약처가 검토한 임상 내용을 보면 2세대 ALK 치료제를 1회 이상 사용한 환자 139명에게 1일 1회 100mg을 경구 투여했다.
1차 평가변수는 독립심사위원회(ICR)의 두개내 객관적반응율(ORR)이 포함된 ORR이었다. 임상에는 여성이 56%, 백인 48%, 아시안 38%가 포함됐고 연령 중앙값은 53세(29~83세)였다. 65세 이상은 16%가 참여했다.
139명 중 67%가 뇌전이 환자였고 앞서 잴코리를 제외한 다른 ALK 치료제를 1차로 투여받은 환자 20%, ALK 2차 치료 47%, 3차 이상 ALK 치료제 사용 환자가 33%였다.

결과를 보면 항암화학요법 투여와 상관없이 1차로 알레센자, 알룬브릭, 자이카디아를 사용한 환자 28명에서 로비큐아는 ICR 평가로 ORR 42.9%(95% CI: 24.5, 62.8)를 기록했다. 완전관해(CR) 1명, 부분반응(PR) 11명이었다. 반응지속기간(DOR)은 5.6개월(95% CI: 4.2, NR), 무진행생존기간(PFS) 중앙값은 5.5개월(95% CI: 2.9, 8.2)이었다.
ALK 치료제를 2차 이상 투여한 환자 111명에서 ORR은 39.6%(95% CI: 30.5, 49.4, CR 1명, PR 42명)로 mDOR 9.9개월(95% CI: 5.7, 24.4), mPFS 6.9개월(95% CI: 5.4, 9.5)로 나타났다.
뇌전이가 있는 환자에서 로비큐아의 두개내 효과도 측정했다.

1차로 ALK를 사용한 환자 9명에서 ORR 66.7%(95% CI: 29.9, 92.5 / CR 2명, PR 4명)를 나타냈지만 두개내 객관적 반응률(iORR)은 결과값까지 도달하지 않았다. ALK를 2차 이상 사용한 환자는 48명이었고 ORR은 52.1%(95% CI: 37.2, 66.7 / CR 10명, PR 15명)이며 iORR은 12.4개월로 나타났다. 아시안인 하위그룹 분석에서 ORR은 49.1%(95% CI: 35.1, 63.2), 비아시아인은 31.5%(95% CI: 21.1, 43.4)였다.
▶화이자가 본 로비큐아 임상 효과
화이자는 ALK 양성을 새로 진단받고 뇌 등 신체 다른 부위로 전이가 일어난 환자 296명을 대상으로 잴코리와 비교 임상을 했다.
1차 평가변수는 PFS였고 로비큐아는 잴코리 대비 암 전이 등 위험을 72% 줄였다. 추적관찰기간 9.3개월(중앙값) 동안 잴코리 투여 환자 절반은 암세포가 퍼진 반면 로비큐아를 투여한 환자 절반 이상이 암세포 증식을 멈췄다. 다만, 로비큐아를 투약한 환자 절반은 아직 확인되지 않았으므로 수명 연장에 효과가 있는지 보기 위해선 시간이 더 필요한 상황이다.
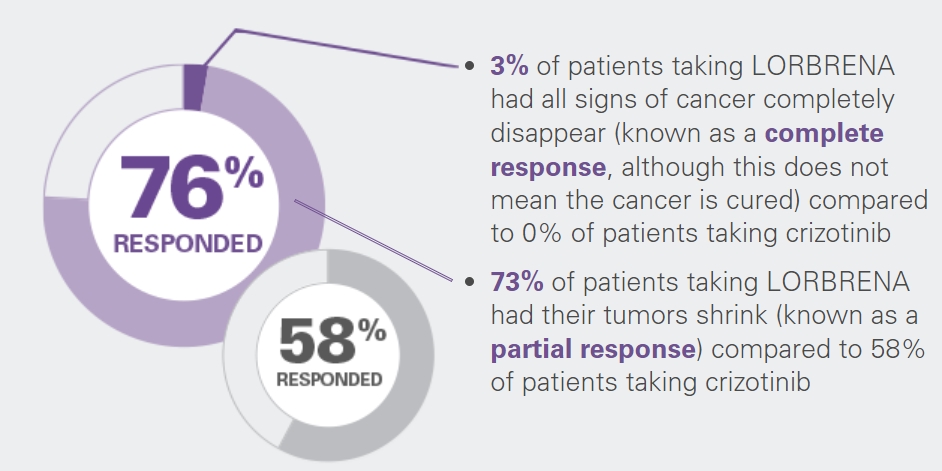
로비큐아를 투여한 환자의 뇌를 포함한 신체 내 종양 수축 등 반응인 ORR을 측정한 결과 76%에서 종양이 줄거나 없어졌다. 로비큐아 투여 환자 중 73%에서 PR이 확인됐고 3%는 CR을 보였다. 잴코리 복용 환자에서 PR은 58%였고 CR은 0%였다. 또한 로비큐아 투여 환자 70%는 12개월 동안 효과가 지속됐다.
해당 임상에 참여한 환자 296명 중 치료 시작점에 뇌종양을 가진 환자는 30명이었다. 30명 중 17명이 로비큐아를 투여받았다.
뇌전이를 가진 17명의 환자를 대상으로 로비큐아의 두개내 효과를 보니 82%가 뇌종양이 줄고 없어졌다. 자세히는 17명 중 12명(71%)에서 CR이 나타났고 2명(12%)은 뇌종양이 부분적으로 축소된 PR이 확인됐다. 잴코리 투여 환자는 13명 중 2명(15%)만 감소 효과를 나타냈다. 로비큐아 두개내 효과를 12개월간 본 결과 효과가 지속된 환자는 79%였지만 잴코리는 0%였다.
관련기사
개의 댓글
댓글 정렬
그래도 삭제하시겠습니까?

