
[팜뉴스=김민건 기자] 지금껏 우리가 알고 있던 약의 개념을 뒤바꾼 '혁신신약'이 연달아 등장하면서 그야말로 새로운 시대가 도래했다. 하지만 우리 사회와 정부 정책은 혁신성을 따라가지 못하고 있다. 희귀질환자와 보호자에게 또 다른 아픔을 남기고 있다.
지난 달 28일 식품의약품안전처는 문제가 되는 유전자를 대체해 원천적으로 희귀질환을 치료하는 척수성 근위축증(SMA) 치료제 '졸겐스마(오나셈노진아베파르보벡)'를 허가했다. 올해 3월에는 개인 맞춤형 항암제 '킴리아(티사젠렉류셀)'가 허가됐다.
최초의 유전자 대체 치료제(Gene replacement therapy)인 졸겐스마는 한 번 투약으로 지속적인 치료 효과를 가진다. 세포·유전자치료제인 킴리아는 대체 치료가 불가한 환자에서 T세포를 채취해 유전자를 재조합하면 암세포를 찾아 사멸한다.
두 치료제는 단 1회 투약으로 다른 치료 옵션이 없는 환자의 생명을 연장시키기에 '원샷 치료제'로 불린다.
그러나 우리 사회는 혁신신약을 받아들일 준비가 되지 않았다.
SMA 환우회 문종민 이사장은 졸겐스마 허가 이후 팜뉴스와 가진 통화에서 "25억원(치료비용)이라는 단어가 언급된 기사가 많이 나갔다. 기사에 달린 댓글 중 응원도 많았지만 그렇지 않은 글도 많아 상처받은 환우들이 굉장히 많다"고 했다. 그는 "(25억원이라는 치료비를)모르는 바는 아니지만 당연히 부담되고 솔직히 무섭다"고도 했다.
지난 2019년 발생한 희귀질환자는 우리나라 인구 0.1%(5만5499명)에 불과하다. 2021년 대한민국에서도 희귀질환에 대한 사회적 인식 미비는 여전하다. 여기에 우리나라 급여 정책은 국민이 내는 돈으로 운영하는 국민건강보험에서 비용을 지불한다.
그렇다보니 '약가'는 매우 민감하고 중요한 이슈일 수밖에 없다. "25억원(졸겐스마), 5억원(킴리아)이나 하냐"며 곱지 않은 시선과 댓글이 달리는 이유다. 문 이사장이 무섭다라는 솔직한 심정을 내비친 이유가 여기에 있을 것이다.
하지만, 혁신신약에서 중요한 것은 실제 혜택을 환자가 볼 수 있느냐다. 바로 건보 급여 적용이 관건이다. 우리 삶이 저마다 다를지라도 치료 받을 기회는 공평해야 한다는 목소리가 들린다.
◆환자 "정말 살고 싶습니다", 혁신신약 평가할 수 없는 정부
지난 달 3일 청와대 국민청원에는 '좀 더 살고 싶습니다, 킴리아 보험 적용'이라는 글이 올라왔다.
40살에 2살 아이를 둔 아빠인 청원인은 "조혈모세포 이식을 해도 항암 불응으로 예후가 좋지 못할 것이란 의사 말을 들었다"며 "킴리아라는 약이 들어오는데 아직 보험적용이 안 돼 4~5억 한다고 하시더라. 4~5억은 생각도 할 수 없어 울음을 흘리는 분들이 많고 저 또한 못한다"고 호소했다.
청원인은 "항암 불응으로 치료법이 없는 경우 킴리아는 살 수 있는 마지막 희망같은 약이다. 앞으로 이런 약들은 승인과 동시에 보험적용이 이뤄졌으면 좋겠다며 많은 분들이 투병 중에 하늘나라로 가고 계시다"고 했다.
그는 "살고 싶습니다. 정말 살고 싶습니다. 솔직히 얼마나 버틸 수 있을지 모르겠지만 약이 승인될 때까지 버텼으면 좋겠다. 간절히 희망의 끈을 놓지 않으려 노력 중"이라고 했다.

희귀질환자들의 희망에도 현재 국내 의약품 급여 정책은 혁신신약의 '혁신성'을 쫒아가지 못한다. 국내에선 혁신신약 가치를 평가할 기준 자체가 없다.
국내 의약품 급여 정책은 치료 가치와 비용-효과를 인정한 의약품만 선별 등재(positive list system)하는 방식이다. 그 이후 약제 급여가 적정한지 평가하고, 제약사와 협상을 거쳐 급여 목록에 등재한다. 이로써 국민이 보험 혜택을 받을 수 있다.
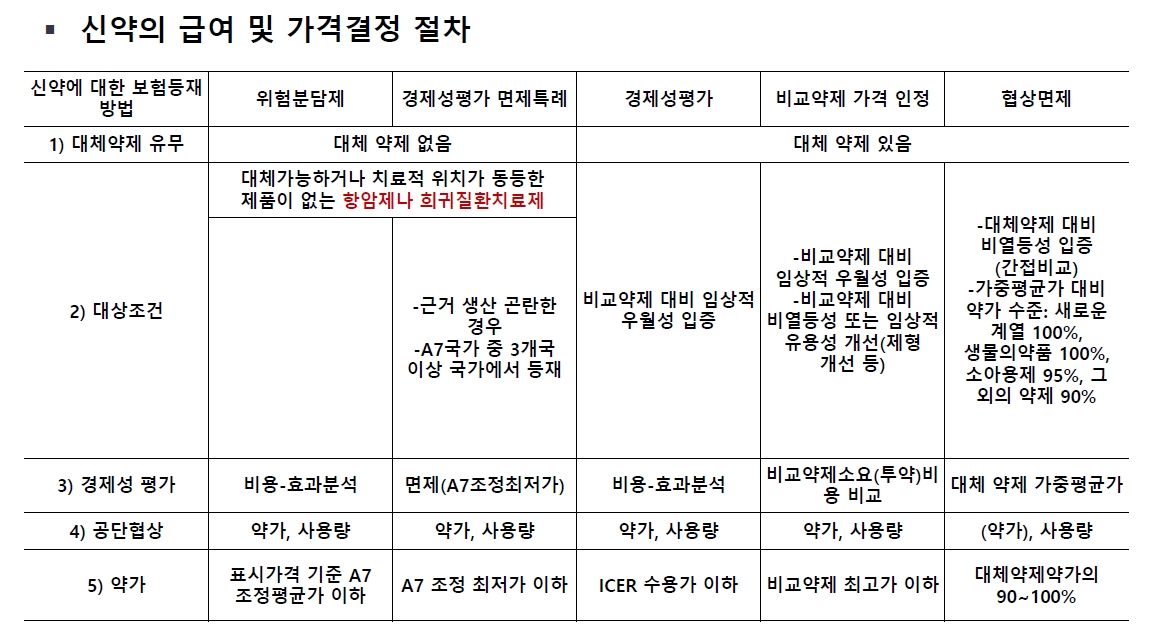
혁신신약을 급여권으로 도입하기 위한 대표적인 제도로 위험분담제(RSA)나 경제성평가 면제특례(이하 경평면제)가 있다. 위험분담제는 해당 치료제가 제약사 주장처럼 정말 효과적이라면 그 부담을 정부와 제약사가 나누는 제도다. 이를 위해선 임상연구와 장기간 추적관찰 데이터로 효과를 입증해야 한다.
경평면제도 희귀질환 200명 미만인 경우에 해당한다. 졸겐스마는 매년 약 20명, 킴리아는 약 30명의 환자가 그 혜택을 받을 것으로 추정될 만큼 극소수다.
혁신신약은 단 1회 치료로 끝나기 때문에 중간에 효과가 떨어졌을 경우 '비용 지불'을 어떻게 할지가 문제다. 또한 환자에서 혁신신약이 효과를 보였는지를 평가할 기준점 자체가 없다. 그러다보니 치료 가치는 물론 비용-효과성을 평가하기 어렵다.
이는 졸겐스마를 허가한 식품의약품안전처가 투여 대상자를 15년간 장기추적조사 하며, 1년 마다 그 내용과 결과를 보고하도록 한 배경이다.
◆졸겐스마와 같지만 다른 SMA 치료제 스핀라자
혁신신약 평가의 어려움은 졸겐스마와 같지만 다른 치료제 스핀라자(뉴시너센) 도입 사례를 통해 비교할 수 있다.
졸겐스마와 동일한 SMA 치료제 스핀라자는 허가 당시 단일 1바이알당 최고가 치료제였다. 정부는 적극적으로 스핀라자 급여를 인정했다.
이를 위해 환급형 위험분담제와 총액제한형, 사전에 투약대상 적정성을 평가받는 사전승인제를 도입했다. 여기에 의료진이 투약 효과를 보고하도록 해 급여 중단이나 지속 여부를 결정하게 했다. 이른바 '하이브리드' 전략이다.
평생 투약해야 하는 스핀라자는 단 1회 치료로 끝나는 졸겐스마와 달리 지속 평가가 가능했기에 가능한 경우였다.
현재 건보 적용을 받는 스핀라자 약가는 약 1억원이다. 투약 첫 해 약 6회를 맞아 6억원 가량 필요하다. 그 다음해부터 매년 3회 투약한다. 이를 10년으로 환산하면 약 36억원이다. 실상 졸겐스마 1회 투약 비용인 25억원(미국 기준) 보다 비싸다.
졸겐스마를 허가하고 사용 중인 해외에서는 '가치 기반 보상' '분할 상환 지급 모델' 등을 도입해 접근성을 확보했다. 단 1회 투약으로 평생 치료 비용보다 혜택을 볼 수 있기 때문이다.
◆의료 불평등 신호탄 쏘아졌다
지난 3월 23일 열린 킴리아 허가 기자 간담회에서 서울대병원 강형진 소아청소년과 혈액종양분과 교수는 "국내에서 킴리아 적응증 대상 환자는 소아암에서 매년 40~50명으로 예상하는데 이제부터 시작일 것"이라고 했다.
강 교수는 "또 다른 암종에서 적응증이 확대 돼 대상 환자가 늘어날 것"이라며 유전자 대체 치료제 같은 혁신신약 사용이 더욱 많아질 것이라고 우려했다.
제약업계에서도 향후 몇년 이내 졸겐스마, 킴리아 같은 혁신신약이 등장할 것으로 보고 있다.
돈이 있으면 살고, 없으면 죽는 의료 불평등 현실에 빨간불이 켜진 상황이다.
앞서 SMA환우회 문 이사장은 "식약처가 허가를 했으면 약에 대한 기본적인 부작용 검증은 마쳤다고 판단한다"며 "같은 국민인데 누구는 보험이 되고, 누구는 안 되는 것보다는 환자에게서 효과가 있다면 비용을 지불하는 것을 제약사가 받아들이고 정부도 진행했으면 좋겠다"고 말했다.
관련기사
개의 댓글
댓글 정렬
그래도 삭제하시겠습니까?

